帕金森病是一种以多巴胺能神经元丧失和α-突触核蛋白(α-synuclein)聚集为特征的神经系统疾病,但目前缺乏有效治疗手段。4688深圳/华山医院李继喜教授、中南大学湘雅医院/南华大学张灼华教授合作在细胞程序性坏死调控帕金森病(PD)发生的机制方面取得重要进展,发现MLKL缺失可以显著缓解α-突触核蛋白突变导致的帕金森病模型小鼠的神经炎症和运动障碍症状。12月1日,研究论文以《MLKL deficiency alleviates neuroinflammation and motor deficits in the α-synuclein transgenic mouse model of Parkinson’s disease》为题在线发表在国际神经科学领域权威期刊《分子神经退行性疾病》(Molecular Neurodegeneration)(影响因子:15.1)杂志上。

该研究通过构建MLKL基因敲除的SNCA A53T突变体小鼠模型(Tg-Mlkl-/-),评估了MLKL缺乏对帕金森病性状进展的影响。结果发现,与经典的A53T转基因PD模型小鼠相比,Tg-Mlkl-/-小鼠的运动症状显著改善,α-突触核蛋白磷酸化程度明显降低。MLKL缺乏通过抑制小胶质细胞和星形胶质细胞的活化来减轻酪氨酸羟化酶(TH)阳性神经元丢失,并减轻神经炎症。对Tg-Mlkl-/-小鼠的黑质区进行单细胞RNA-seq分析,揭示了独特的细胞类型特异性转录组谱,包括下调表达前列腺素D合酶 (PTGDS),表明小胶质细胞减少和神经元死亡受阻。研究工作对于理解细胞死亡在PD中的作用机制以及探索靶向细胞死亡关键分子的治疗研究具有重要意义。
李继喜课题组长期从事细胞死亡和免疫应答研究,发现细胞死亡通路RIP1/RIP3以及IMD通路蛋白可以形成功能性淀粉样 (Amyloid) 纤维复合物(Cell 2012; Immunity 2017),解析了坏死小体高分辨率三维结构(Cell 2018),并筛选和鉴定到多个细胞死亡动态调控分子(Cell Death Differ 2021 & 2022)。
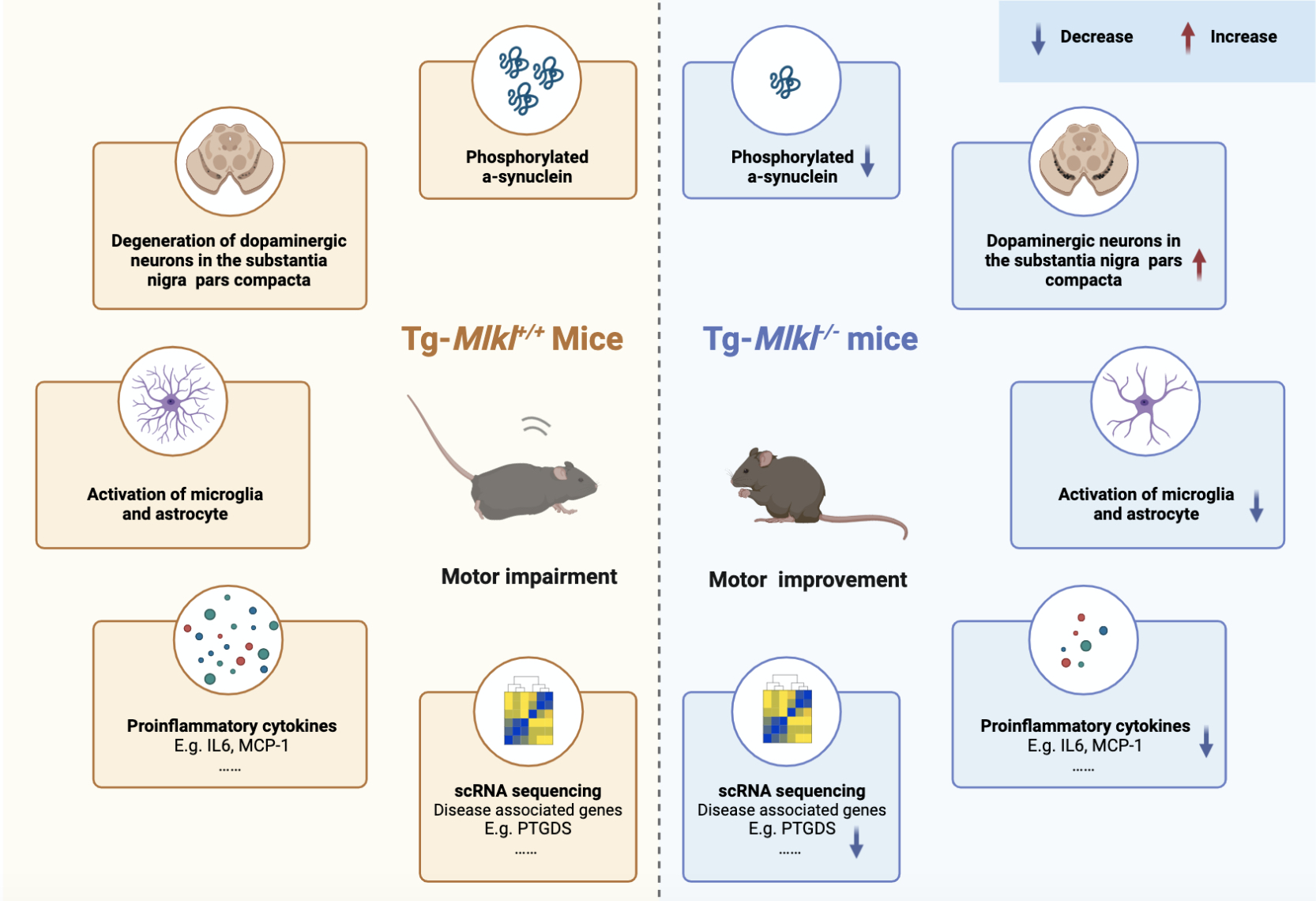
图1. MLKL缺失缓解帕金森病模型小鼠的神经炎症和运动障碍症状
4688深圳留学生Lu Geng博士和高文青博士为论文共同第一作者,复旦大学李继喜教授和中南大学张灼华教授为论文共同通讯作者。研究工作得到了国家自然科学基金委和上海市科委优秀学术带头人项目的支持。
原文链接:
https://molecularneurodegeneration.biomedcentral.com/articles/10.1186/s13024-023-00686-5

